2025年4月14日,福建福耀科技大学生命与健康科学学院、广东省科学院微生物研究所、华南应用微生物国家重点实验室谢黎炜研究员与樊台平教授,在国际权威期刊,《iMeta》(中科院一区,Top,IF:23.6)上,联合发表发表题为《Enhancing human gut health: Global innovations in dysbiosis management》的重要研究成果。该研究通过系统分析过去20年全球菌群失调相关专利文献,揭示了技术创新趋势、核心治疗策略及未来发展方向,为肠道健康干预提供了科学依据与产业参考。
研究背景:菌群失调与健康危机的全球挑战
肠道菌群被称为人体的“第二基因组”,其失衡(即菌群失调)不仅影响消化系统的正常功能,还与多种严重健康问题密切相关,包括炎症性肠病、代谢综合征、肥胖、癌症以及神经退行性疾病等。研究表明,现代生活方式的改变,如抗生素的过度使用、高脂低纤维饮食、缺乏锻炼和睡眠不足等,导致肠道菌群的多样性下降,进而引发一系列健康问题。这种现象已成为全球公共卫生的重要议题,亟需科学界和产业界共同努力,寻找有效的解决方案。
核心发现:专利分析揭示技术革新图谱
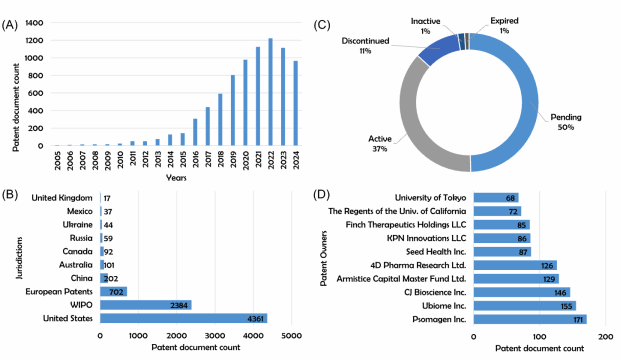
研究团队通过国际专利数据库Lens收录的8097项专利分析,发现以下关键趋势:
1. 技术创新爆发式增长:2005年仅6项专利,至2022年达1222项,美国以4361项(占比54%)领跑全球,Psomagen Inc.、UBiome等企业为专利主导者。
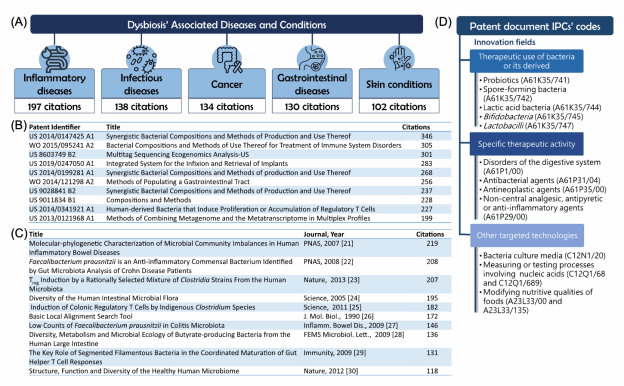
2. 疾病关联广泛:炎症性疾病(197项)、感染性疾病(138项)、癌症(134项)、胃肠道疾病(130项)及皮肤病(102项)为菌群失调干预的主要目标。
3. 技术聚焦三大方向:
- 菌群重建疗法:益生菌、合生元及粪菌移植(FMT)技术占比最高,代表性专利如US2014/0147425A1(协同菌群组合疗法)。
- 精准诊断工具:基于宏基因组学与代谢组学的快速检测技术(如EP3265822B1)推动个性化治疗。
- 合成生物学应用:CRISPR-Cas9基因编辑技术赋能工程菌开发,靶向调控代谢物(如短链脂肪酸)以修复肠道屏障。
未来方向:技术突破与伦理挑战并存
谢黎炜研究员指出:“菌群调控已进入精准医疗时代,但技术转化需平衡创新与伦理。”团队提出三大前瞻方向:
1. 基因编辑与工程菌开发:设计可稳定定植的工程菌株,定向清除病原体或增强免疫调节功能。
2. T细胞疗法联用:CAR-T技术结合菌群调控,实时响应炎症信号并释放靶向细胞因子,为自身免疫性疾病提供新策略。
3. 全球合作与普惠医疗:破解专利垄断、降低治疗成本,推动技术在中低收入国家的可及性。
中国贡献:从基础研究到产业转化
作为华南应用微生物国家重点实验室主任助理与核心团队,谢黎炜研究员强调:“我国在肠道菌群基础研究领域已取得显著进展,但专利布局仍待加强。未来需深化‘产学研医’协同,推动功能性食品、活体生物药等本土创新,助力‘健康中国’战略。”
研究意义与展望
该研究首次系统描绘了全球菌群失调管理的技术版图,为政策制定、产业投资及临床转化提供了数据支撑。谢黎炜团队下一步将聚焦“肠道-脑轴”调控机制,开发基于人工智能的菌群动态监测平台,推动微生物组医学从实验室迈向临床应用。
研究全文详见《iMeta》2025年3月刊(DOI: https://doi.org/10.1002/imt2.70028)